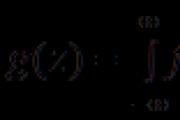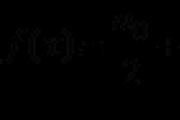রাসায়নিক বিক্রিয়ায় নীল গ্যাসের আয়তন। অ্যাভোগাড্রোর আইন
গ্যাসের মতো বক্তৃতা শিবির। অ্যাভোগাড্রোর আইন। গ্যাসের মোলার আয়তন।
বক্তৃতা তিনটি সমষ্টিগত মিলগুলিতে পুনর্ব্যবহৃত করা যেতে পারে - কঠিন, বিরল এবং বায়বীয়। অংশ, যে সংখ্যা, কঠিন বক্তৃতা গঠিত হয়, এটি নিজেদের মধ্যে mіtsno pov'yazanі করতে, যে কঠিন বক্তৃতা, তারা একটি একক ফর্ম গঠন করে। কঠিন দেহের অংশগুলি পরমাণু, অণু, আয়ন হতে পারে, যা স্ফটিক কাঠামো তৈরি করে। Qi chastki kolivayutsya একটি ছোট প্রশস্ততা মারধর vuzlіv স্ফটিক ґrat সঙ্গে। স্থানীয় অঞ্চলে, অংশগুলি এক থেকে এক দুর্বলভাবে বাঁধা থাকে এবং একটি বড় পার্থক্য করার জন্য অতিরিক্ত পোশাক পরা যেতে পারে। এই কারণে, plinnist এবং বিচারকদের ফর্ম ফুলে, যার মধ্যে দুর্গন্ধ পরিচিত হয়।
কঠিন অবস্থা থেকে বক্তৃতার স্থানান্তর খুব কমই পরিলক্ষিত হয় যখন উত্তপ্ত হয়, যার ফলস্বরূপ কণাগুলির বিভাজনের প্রশস্ততা ধীরে ধীরে বৃদ্ধি পায়। যখন তাপমাত্রা বেশি হয়, তখন বক্তৃতার কণাগুলি zdatnost দিয়ে ফুলে যায়, burr এর গিঁটগুলিকে অভিভূত করে, গলে যাওয়া পরিলক্ষিত হয়। ঠাণ্ডা হলে, navpaki, rіdini-এর অংশগুলি zdatnіst সরাতে এবং গানের অবস্থানে ঠিক করে, বক্তৃতাকে দৃঢ় করে। সর্বশ্রেষ্ঠ মনের জন্য, রিডিনি, একটি নিয়ম হিসাবে, আণবিক জীবন পরিশ্রম করে। উচ্চ তাপমাত্রায়, রিডিনির গঠন ভিন্ন হতে পারে (লবণ এবং ধাতু গলে যাওয়া)।
অণুগুলির মধ্যে মিথস্ক্রিয়া প্রচুরভাবে দুর্বল, আয়নিক স্ফটিক কাঠামোতে আয়নের মধ্যে কম; পারমাণবিক কাঠামোতে সমযোজী বন্ধন দ্বারা আবদ্ধ পরমাণু; ধাতব আয়ন, ধাতব কাঠামোতে ইলেকট্রন গ্যাস দ্বারা আবদ্ধ।
সাহসী নাম করার জন্য একটি দৃঢ় এবং বিরল বক্তৃতা শিবির ঘনীভবন কল. ঘনীভূত ইস্পাত মধ্যে বক্তৃতা পুরুত্ব আনুমানিক 0.5 - 22.5 গ্রাম / সেমি 3 এর সীমানায় পরিবর্তিত হয়। গ্যাসের মতো স্টেশনে বক্তৃতা উল্লেখযোগ্যভাবে কম বেধ থাকতে পারে - 10 -2 - 10 -3 গ্রাম / সেমি 3 এর কাছাকাছি। গ্যাস-সদৃশ মিলের স্থানান্তরটি ঘনীভূত মিলের (কঠিন পদার্থের ফুটন্ত, কঠিন বক্তৃতার পরমানন্দ) স্পিচগুলিকে গরম করার কারণে ঘটে। বাকশক্তির সর্বশ্রেষ্ঠ মনের জন্য গ্যাসের মতো অণু দ্বারা গঠিত।
গ্যাসের মতো অবস্থায় যাওয়ার সময়, বক্তৃতা কণাগুলি আন্তঃআণবিক মিথস্ক্রিয়া শক্তি যোগ করে। Obsyag, যা গ্যাস দখল করে, যা প্রকৃতপক্ষে, গ্যাসের অণুর মধ্যে মুক্ত স্থানকে অস্পষ্ট করে, যা এলোমেলোভাবে ভেঙে পড়ে। এই বিস্তৃতির আকার তাপমাত্রা এবং ভাইস দ্বারা নির্ধারিত হয়। যখন আমরা obsyagom, নিজেদের অণু দ্বারা দখল, আমরা বিদ্রোহ করতে পারেন. তারা চিৎকার করছে অ্যাভোগাড্রোর আইন :
বিভিন্ন গ্যাসের সমান অঙ্গীকার একই মনের জন্য একই সংখ্যক অণু রয়েছে।
অ্যাভোগাড্রো চিৎকারের আইন দুটি প্রধান ফলাফল .
প্রথম পরিণতি
একই মনের জন্য যেকোন ধরনের গ্যাসের এক তিল একই অঙ্গীকার ধার করে। Tsey obsyag বলা হয় মোলার গ্যাসের চাপ ( ভি মি ) , যা m 3 / mol (প্রায়শই dm 3 / mol মধ্যে) vimiryuetsya। গ্যাসের মোলার বাধ্যবাধকতা একই পরিমাণে গ্যাসকে বাধ্য করার জন্য আরও উন্নত:
Vіdomo, scho মান V m vіd মনে পড়ে (তাপমাত্রা, tysk)। কাজটি সম্পূর্ণ করার জন্য, V m-এর মান মনে রাখা প্রয়োজন স্বাভাবিক মন (n.o.s.) - বায়ুমণ্ডলীয় চাপ (101.3 kPa) এবং বরফের তাপমাত্রা (0 0 C বা 273.15 K)।
স্বাভাবিক মনের জন্য V m \u003d 22.4 dm 3 / mol, বা
CI ইউনিটে 0.0224 m 3 / mol।
আরেকটি পরিণতি
গ্যাসের প্রস্থ (বা একই গ্যাসের ভর) গ্যাসের মোলার ভর হিসাবে একত্রিত হয়।
আপনি যেমন আয়না থেকে এটি দেখতে পারেন. একই বাধ্যবাধকতার বিভিন্ন গ্যাসের দুটি অংশ নিয়ে আসুন (একই মনের জন্য ভিমিরিয়ানের বাধ্যবাধকতা)। আমরা তাদের জানি:
সেটিং їх ভর:
Yakshcho vikoristovuvat schіlnіst:
অ্যাভোগাড্রোর আইন n 1 \u003d n 2 এর পিছনে, দেখুন:
মোলার ভরের পরিবর্তনে গ্যাসের পুরুত্বের পরিবর্তনকে বলা হয় একটি গ্যাস অপরটিতে বহন ক্ষমতা ( ডি ) D - মানটি অনির্ধারিত।
ডি এবং একটি গ্যাসের মোলার ভর জানা, অন্য গ্যাসের মোলার ভর জানা সহজ:
; M1 = M2 × ডি.
আবেদন
M(x) = M(H2) × D=2 × 8.5 = 17 গ্রাম/মোল
এই ধরনের মোলার ভর থেকে গ্যাস - অ্যামোনিয়া NH 3 .
একটি নির্দিষ্ট গ্যাস-সদৃশ কার্বোহাইড্রেটের শক্তি দুটির জন্য আরও ব্যয়বহুল দেখানো হবে। আপনার মোলার ভরকে কার্বোহাইড্রেটে পরিবর্তন করুন।
গড় মোলার ভর 29 গ্রাম/মোল বলে মনে হচ্ছে।
M(x) = M(p.) × D=29 × 2 = 58 গ্রাম/মোল
এই ধরনের মোলার ভরযুক্ত কার্বোহাইড্রেট হল Z 4 H 10 বিউটেন।
উল্লেখ্য যে মোলার ভর 29 এর কম সহ গ্যাসগুলি প্রতি পুনরাবৃত্তি সহজ, 29 এর বেশি গুরুত্বপূর্ণ।
rozrahunkovyh গাছপালা, নাইট্রোজেন, অম্লতা এবং অন্যান্য গ্যাসের তথ্য থাকতে পারে। এই ক্ষেত্রে, মোলার ভরের মানের জন্য, নাইট্রোজেন (28 গ্রাম/মোল), টক (32 গ্রাম/মোল) ইত্যাদির মতো মোলার ভর দ্বারা সান্দ্র বেধকে গুণ করা প্রয়োজন।
অ্যাভোগাড্রোর আইন রাসায়নিক গবেষণায় ব্যাপকভাবে ব্যবহৃত হয়। গ্যাসের জন্য Oskіlki বক্তৃতা সংখ্যার সমানুপাতিক, তারপর সমান বিক্রিয়ায় সহগ, যা প্রতিক্রিয়াশীল বক্তৃতার সংখ্যা প্রতিফলিত করে, হস্তক্ষেপকারী গ্যাসের অনুপাতের সমানুপাতিক। স্পষ্টতই, scho obsyagi ময়ূত কিন্তু একই মনের জন্য vimiryan.
বাট
spalling 2 dm জন্য কিছু ধরনের টক প্রয়োজন হবে 3 প্রোপেন? Vymiryan obyagi জন্য n. y
H 3 H 8 + 5O 2 3CO 2 + 4H 2 O।
অ্যাভোগাড্রোর আইন থেকে, এটি স্পষ্ট যে বিভিন্ন গ্যাসের সমান সংখ্যক অণুর সমান হওয়া উচিত, এবং স্পষ্টতই, একই সংখ্যক বক্তৃতা মোল। আসুন 1 dm3 পর্যন্ত প্রোপেন পাই। Todi, একটি সমান প্রতিক্রিয়া থেকে, 1 dm 3 প্রোপেন স্ক্যাল্ডিংয়ের জন্য 5 dm 3 টক, এবং 2 dm 3 (দুই লিটার) - 10 dm 3 প্রো 2 প্রয়োজন।
রসায়ন
গ্লোবাল কেমিস্ট্রি
রসায়নের মৌলিক ধারণা, আইন এবং তত্ত্ব
রাসায়নিক বিক্রিয়ায় নীল গ্যাসের আয়তন। অ্যাভোগাড্রোর আইন
গে-লুসাকের অর্থের আইন
সাধারণ বক্তৃতার গানে গাজীরা একে অপরের সাথে প্রতিক্রিয়া জানায়। 1808 সালে পি. জে.এল. গে-লুসাক নিম্নলিখিত নিয়ম প্রতিষ্ঠা করেছেন: বিক্রিয়ায় যে পরিমাণ গ্যাস প্রবেশ করে বিক্রিয়ায় সেই গ্যাসের মতো দ্রব্যগুলির একটি থেকে একটিকে ছোট সংখ্যা হিসাবে দেখা যায়।.
Vіdkritiy vchenim রসায়ন ইয়াক মধ্যে vіdomy আইন আয়তনের আইনখ. যোগব্যায়ামের জন্য, বিক্রিয়ায় অংশ নেওয়া গ্যাসগুলিকে একই তাপমাত্রা এবং চাপে রাখতে হবে।
Vіdnoshennya obsyagіv gazіv, রাসায়নিক বিক্রিয়ায় প্রবেশ করতে scho, সহগ সমান vіdpovіdat, উদাহরণস্বরূপ: .
এই ক্ষেত্রে, 3 ভলিউম জল 1 ভলিউম নাইট্রোজেনের সাথে বিক্রিয়া করে, যার ফলে 2 ভলিউম অ্যামোনিয়া দ্রবীভূত হয়, যাতে স্বতঃস্ফূর্ততা দেখানো হয়।
ম্যানেজার। 2 মি 3 নাইট্রোজেনের জন্য প্রয়োজনীয় জল বিক্রিয়া কী?
সমাধান
সমান প্রতিক্রিয়া থেকে, এটি দেখা যায় যে জলের আয়তন দায়ী কিন্তু নাইট্রোজেনের আয়তনের জন্য 3 গুণ বেশি:
obsyag জল m3.
অ্যাভোগাড্রোর আইন
সহজ spіvvіdnoshenі mіzh vzyagyah বিক্রিয়া গ্যাস vikoristovuyut Avogadro এর আইন ব্যাখ্যা করতে: একই মনের (তাপমাত্রা এবং চাপ) জন্য বিভিন্ন গ্যাসের সমান বন্ধনে একই সংখ্যক অণু থাকে।আমি অ্যাভোগাড্রোর আইনকে দুবার চিৎকার করতে দেইনি ta:
1) একই মনের জন্য যে কোনও ধরণের গ্যাসের এক তিল একই বাধ্যবাধকতা ধার করে।
স্বাভাবিক মনের জন্য (n.a.), তারপর 273 K এবং 101.3 kPa (1 atm) তাপমাত্রায়, যেকোনো গ্যাসের 1 মোল একটি আয়তন নেয়, 22.4 লিটারের সমান। Tsei obsyag কল মোলার গ্যাস i মানে l/mol.
মোলার বন্ধন সূত্র দ্বারা আলগা করা যেতে পারে
.
2) একটি ধ্রুবক চাপের সাথে, গ্যাসের ফাঁকের তাপমাত্রা এক মোলার ভরের কম।
Tse আপনি ভুল বোঝার অনুমতি দেয় প্রবেশযোগ্য বেধঅন্য উপায়ে প্রথম গ্যাস:
,
ডি ডি- দৃশ্যত শিলনিস্ট, যেমনটি দেখায়, একই সময়ে প্রথম গ্যাসটি একই মনের জন্য অন্যটির জন্য গুরুত্বপূর্ণ।
প্রায়শই, ভাইকোরিস্ট গ্যাসের মাধ্যমে জল দেখতে সক্ষম হয়। টোডি:
; .
যে কোনো গ্যাসের জন্য একটি পুরু ঝোপ আলগা করা সম্ভব।
যার ভিকোরিস্তান সামগ্রী বিতরণ পদ্ধতিগত সহকারী"রসায়নের নবচান্ন্যা রোজভ্যাজান্নু সমস্যা"। লেখক - প্রশাসক: সর্বোচ্চ বিভাগের রসায়নের শিক্ষক, শিক্ষা ইনস্টিটিউটের পদ্ধতিবিদ "গ্রোডনো শহরের জিমনেসিয়াম নং 1" টলকচ এল ইয়া।; শিক্ষা ইনস্টিটিউটের প্রাথমিক-পদ্ধতি বিভাগের পদ্ধতিবিদ "Grodno OIPK এবং PRR এবং SV" Korobova N.P.
গ্যাসের মোলার ভলিউমের সংখ্যা গণনা।
গ্যাসের বিশিষ্ট ঝোপের গণনা।
নীল গ্যাসের আয়তন
একই মনের জন্য যেকোন ধরণের গ্যাসের এক তিল একই এক দখল করে। সুতরাং, স্বাভাবিক মনের জন্য (n.o.),tobto 0 °সে তাপমাত্রায় এবং স্বাভাবিক বায়ুমণ্ডলীয় চাপ, যা 101.3 kPa, যে কোনো গ্যাসের এক মোল আয়তন দখল করে22.4 dm3।
বিন্যাসআমি গ্যাসকে একটি নির্দিষ্ট রাসায়নিক পরিমাণে বক্তৃতা করতে বাধ্য করি - মান, যেমন এটি বলা হয়মোলার গ্যাসের চাপ (ভিএম):
ভিএম = ভি/ ndm 3, তারাভি = ভিএম · n
চয়ন করার জন্য: হালকা বা সবচেয়ে গুরুত্বপূর্ণ গ্যাসটি অন্যান্য গ্যাসের সমান, তাদের বেধ সমান করার জন্য এটি যথেষ্ট:
r 1 / r 2 = M 1 V 1 / M 2 V 2 = M 1 / M 2 = D 2.প্ররোচিত ভিরাজের দৃষ্টিকোণ থেকে, এটি পরিষ্কার: গ্যাসের প্রস্থ সমান করা, তাদের মোলার ভরের সমানতা অর্জন করা।
একটি গ্যাসের মোলার ভরের সাথে অন্য গ্যাসের মোলার ভরের অনুপাত হল মান, যাকে বলা হয়
উপলব্ধিযোগ্য স্থান ( ডি 2 ) একটি গ্যাসের সাথে আরেকটি গ্যাস।একটি গ্যাসের শক্তি অন্যটিতে জেনে আপনি মোলার ভর গণনা করতে পারেন:
এম
1 = এম 2 · ডি 2 .আপনি যদি গ্যাসের যোগফল দেখতে পান, তাহলে এই "মোলার ভর" 22.4 লিটারের আয়তনের ভরের সমান। Tsya মান সংখ্যাগতভাবে আরও উন্নত:
M pov. = 29 গ্রাম/মোল
স্পষ্টতই, অ্যাভোগাড্রোর সূত্র পর্যন্ত, শান্ত মনের জন্য বিভিন্ন গ্যাসের একই সংখ্যক অণু একই পরিমাণ নেয়।
এই এক থেকে, আরেকটি পরিণতি স্পষ্ট হয়.
ধ্রুবক তাপমাত্রা এবং চাপে, গ্যাসগুলি এক থেকে এক প্রতিক্রিয়া করতে শুরু করে, এবং গ্যাসের মতো পণ্যগুলির পরিমাণও, যা ছোট সংখ্যার মতো স্থির হয়।
এই আইনটি গে-লুসাক দ্বারা গ্যাসের আয়তনের আইন হিসাবে প্রণয়ন করা হয়েছিল। এইভাবে, যদি একটি রাসায়নিক বিক্রিয়া তার অংশ নেয়, বা গ্যাসের মতো বক্তৃতা বেরিয়ে আসে, তবে সমান প্রতিক্রিয়ার জন্য নীলের ভলিউম ইনস্টল করা সম্ভব।
Obsyagi গ্যাস, যা তারা প্রতিক্রিয়া, এই বক্তৃতা রাসায়নিক পরিমাণের সমানুপাতিক:
V 1 / V 2 = n 1 / n 2 tobto. V 1 এবং V 2
সমান বিক্রিয়ার সংখ্যাগতভাবে সমান সহগ।উদাহরণ 1. বেলুনে 0.5 কেজি চেপে রাখা জল থাকে। কি ভলিউমএত বড় পরিমাণ পানি ধার? ধুয়ে ফেলস্বাভাবিক
সমাধান:
1. রাসায়নিক পরিমাণ গণনা করুন
জল, বেলুনে কি প্রতিশোধ নেবেন:এন
(H 2) \u003d 500/2 \u003d 250 (mol), de M (H 2) \u003d 2 g/mol।2. স্বাভাবিক মনের জন্য Oskіlki যেকোনো গ্যাসের 1 মোল মোট 22.4 লাগে
dm 3, তারপরভি = ভিএম · n, ভি( এইচ 2 ) = 22,4 * 250 = 5600 (dm 3)
Vidpovid: 5600 dm 3
বাট 2। অ্যালুমিনিয়াম-মিড অ্যালয়ের কোন গুদাম (%-এ), যেমন 1 গ্রাম অতিরিক্ত আয়োডিন হাইড্রোক্লোরিক অ্যাসিড পরীক্ষা করার সময়, 1.18 l দেখা গেছেজল?
সমাধান:
1. শুধুমাত্র অ্যালুমিনিয়াম অ্যাসিডের সাথে বিক্রিয়ায় প্রবেশ করতে পারেসমান লিখুন:
2A1 + 6HC1 = 2A1C1 3 + 3এইচ 2
2mol 3mol
2. গণনাযোগ্য রাসায়নিক পরিমাণজল:
n(এইচ 2 ) = 1.18/22.4 = 0.05 (mol)
3. প্রতিক্রিয়ার উপর ভিত্তি করে, আমরা অ্যালুমিনিয়ামের ভর গণনা করি,খাদ মধ্যে কি লুকান:
3 mol 2 mol অ্যালুমিনিয়াম
0.05 মোল জল দেখতে, প্রতিক্রিয়া হিসাবে যদিএক্সমোল অ্যালুমিনিয়াম
x \u003d 0.05 2/3 \u003d 0.033 (mol),
মি( আল) = 0.035 27 = 0.9 (g), de M(Al) = 27 গ্রাম/মোল
5. গণনাযোগ্য ধাতুতে অ্যালুমিনিয়ামের ভর ভগ্নাংশ:
w(এl) = মি ( আল ) / মি (খাদ) , w( A1) = 0.9/1 = 0.9 চি 90%।
টোডি ভর ভগ্নাংশ মিডি খাদ 10%
প্রকার: 90% অ্যালুমিনিয়াম, 10% মিডি
উদাহরণ 3। উল্লেখযোগ্যভাবে পার্থক্যযোগ্য শক্তি: ক) আমি এটি পুনরাবৃত্তি করব,খ) কার্বন ডাই অক্সাইড জল।
সমাধান:
1. টকের টক দেখলেই বোঝা যায়:
ডি povit (প্রো 2) =এম(প্রো 2)/এম (pov.) = 32/29= 1,1.
2. দ্বারা আমরা কার্বন ডাই অক্সাইডের উপস্থিতি দেখতে পারিজল
ডি H2 (CO 2) =এম(Z 2 )/এম(H 2) \u003d 44/2 \u003d 22।
Vidpovid: 1.1; 22
বাট 4। 0.5 মোল টক, 0.5 মোল জল যুক্ত গ্যাসের আয়তন নির্ধারণ করুনএবং কার্বন ডাই অক্সাইডের 0.5 মোল।
সমাধান:
1. আমরা গ্যাসের সমষ্টির রাসায়নিক পরিমাণ জানি:
n(সুমিশ) \u003d 0.5 + 0.5 + 0.5 \u003d 1.5 (mol)।
2. মোট গ্যাসের পরিমাণ গণনা করুন:
ভি(sumish) \u003d 22.4 1.5 \u003d 33.6 (dm 3)।
প্রস্থ: 33.6 dm 3 যোগফল
উদাহরণ 5। 11.2 মিটার থুতু ফেলার সময় নির্গত কার্বন ডাই অক্সাইডের আয়তন গণনা করুন 3 মিথেন CH 4।
সমাধান:
1. মিথেনের দহনের রাসায়নিক বিক্রিয়া লিখ:
CH 4 + 2O 2 \u003d CO 2 + 2H 2 O
1 আঁচিল1 আঁচিল
1 মি 3 1 মি 3
2. কার্বন ডাই অক্সাইডের পরিমাণ গণনা করতে, আমরা অনুপাত যোগ করি এবং পরিবর্তন করি:
ঘুমানোর সময় 1 m 3 CH 4 weide 1 m 3 2
ঘুমানোর সময় 11.2 মি 3 CH 4 viide x m 3 2
x \u003d 11.2 1/1 \u003d 11.2 (m 3)
ভিডপোভিড: 11.2 মি 3 কার্বন - ডাই - অক্সাইড
উদাহরণ 6. চাপা গ্যাস সংগ্রহের জন্য একটি ইস্পাত সিলিন্ডার 8 কেজির বিরল টক ভরে ভরা ছিল।
কোন obsyag একটি গ্যাস-মত স্টেশন (n.o.) থেকে গ্যাস ধার করেছে?
সমাধান:
1. বিরল টকের রাসায়নিক পরিমাণ গণনা করুন:
n( ও 2 ) = 8000/32 = 250 (mol)।
2. গ্যাসের মতো অ্যাসিডের হিসাব:
ভি( ও 2 ) \u003d 22, 4 250 \u003d 5600 dm 3।
Vidpovid: 5600 dm 3
উদাহরণ 7. 1 মিটার আয়তন দ্বারা ভর গণনা করুন 3 (n.o.), যা নাইট্রোজেনের 78 ভলিউম, 21 - টক, 1 - আর্গন (অন্যান্য গ্যাসের ক্রাইম)।
সমাধান:
1. Vyhodyachi z zavdannya, obsyagi gazіv vіtrі vіdpovіdno dorovnyuyut:
ভি( এন 2 ) \u003d 1 0.78 \u003d 0.78 m 3;
ভি(প্রো 2) \u003d 1 0.21 \u003d 0.21 m 3
ভি(এr) \u003d 1 0.01 \u003d 0.01 m 3।
2. ত্বকের গ্যাসের রাসায়নিক পরিমাণ গণনা করুন:
n( এন 2 ) \u003d 0.78 / 22.4 10 -3 \u003d 34.8 (mol),
n(প্রো 2) \u003d 0.21 / 22.4 10 -3 \u003d 9.4 (mol),
n(এr) \u003d 0.01 / 22.4 10 -3 \u003d 0.45 (mol)।
3. গ্যাসের ভর গণনা করুন:
মি(এন 2 ) = 34.8 28 = 974 (ছ),
মি(প্রো 2 ) = 9.4 32 = 30 (g),
মি(এr) = 0.45 40 = 18 (ঘ)।
4. প্রতিবার ভর গণনা করুন:
মি(পুনরাবৃত্তি) \u003d 974 + 301 + 18 \u003d 1293 (g) বা 1.293 কেজি।
ওজন: প্রতিদিন 1.293 কেজি
উদাহরণ 8। যখন evdiometrі মধ্যে podpalyuvanni 0.1 মি একটি ভলিউম সঙ্গে টক এবং জল 3 মোট যোগফল 0.09 মি দ্বারা পরিবর্তিত হয়েছে 3 .
ইয়াকি প্রতিশ্রুতি দেয়জল এবং টক ছিল প্রস্থান সুমিশি, গ্যাস মত, কি বাকি ছিল, জ্বলন্ত (n.o.)?
সমাধান:
1. সমান প্রতিক্রিয়া লিখুন:
2H 2 + প্রো 2 = 2H 2 প্রো
2 মোল 1mol 2mol
2. এটা সুস্পষ্ট যে গ্যাসগুলি যে প্রতিক্রিয়ায় প্রবেশ করেছে।
প্রতিশ্রুতিবদ্ধ গ্যাসের ব্যাগটি মিষ্টি জলের রাহুঙ্কার জন্য ছুটে গিয়েছিল, যেখানে গ্যাসগুলি, যা প্রতিক্রিয়ায় প্রবেশ করেছিল, 0.09 মিটারে পৌঁছেছিল 3 .
কারণ গ্যাসি 2:1 হারে একটি বিক্রিয়ায় প্রবেশ করুন, তারপর 0.09 মি থেকে 3 দুটি অংশ
জলের উপর পড়ে, এবং একটি - চুম্বন উপর বাবা, একটি প্রতিক্রিয়া আছে
0.06 মি প্রবেশ করেছে 3 জল এবং 0.03 মি 3 টক
3. মোট পরিমাণে গ্যাসের পরিমাণ গণনা করুন।
কারণ গ্যাস, যদি এটি উপচে পড়ে, জ্বলতে থাকে, তাহলে পুরো দিনটি 0.01 মি 3 .
ভি(এইচ 2 ) = ০.০১ + ০.০৬ = ০.০৭ (মি 3 ) বা 70 লি,
ভি(প্রো 2 ) = 0.1 - 0.07 = 0.03 (মি 3 ) বা 30 লি.
পরামর্শ: 70 লিটার জল, 30 লিটার টক
উদাহরণ 9। 56 লিটার আর্গন এবং 28 লিটার নাইট্রোজেন (n.o.) পর্যন্ত যোগ করা গ্যাসের মিশ্রণে জলের পরিমাণের মধ্যে পার্থক্য কী?
সমাধান:
1. Vyhodyachi z vyznachennya vіdnoї gustina gazіv,
ডি এইচ 2 = এম (পাগল) / এম(এইচ 2 ).
2. গ্যাসের যোগফলের রাসায়নিক পরিমাণ এবং ওজন গণনা করুন:
n(আর) = 5.6/22.4 = 2.5 (mol);
n(এন 2 ) = 28/22.4 = 1.25 (mol);
n(sumish) \u003d 2.5 + 1.25 \u003d 3.75 (mol)।
মি(আর) = 2.5 40 = 100 (g),
মি(এন 2 ) = 1,25 28 = 35 (g),
মি(sumish) \u003d 100 + 35 \u003d 135 (g), কারণ
এম (এr) = 40 গ্রাম/মোল, এম (এন 2 ) = 28 গ্রাম/মোল।
3. মোলার ভর যোগফল গণনা করুন:
M(sumish) = মি (পাগল) / n (পাগল) ;
M (সুমিশ) \u003d 135 / 3.75 \u003d 36 (g/mol)
4. পানিতে মোট গ্যাসের পরিমাণ গণনা করুন:
ডি এইচ 2 = 36/2 = 18.
তারিখ: 18
বাট 10। আপনি কি টক (এনও) ভরা তিন লিটার ব্যান্টজে 3 গ্রাম কাঠের ভুগিল পোড়াতে পারেন?
সমাধান:
1. পর্বত ভুগিলের সমান প্রতিক্রিয়া লেখ:
ডব্লিউ + প্রো 2 = তাই 2
1mol 1mol
2. ভুগিলের রাসায়নিক পরিমাণ গণনা করুন:
n(সঙ্গে) = 3/12 = 0.25 (mol), তাই M (C) \u003d 12 g/mol।
বিক্রিয়ার জন্য প্রয়োজনীয় টকের রাসায়নিক পরিমাণও সমান হবে 0.25 মোল
3. 3 গ্রাম ভদকা স্প্যালিং করার জন্য প্রয়োজনীয় টকের পরিমাণ গণনা করুন:
ভি(ও 2 ) = 0,25 22.4 = 5.6(l)।
4. Oskіlki গ্যাস জাহাজের ভলিউম ধার করে, একই ওয়াইনে এটি জানা যায়, є 3 লিটার অ্যাসিড। ওটজে, কিলকোস সেলাই করবেন না spalyuvannya 3 গ্রাম vugillya জন্য।
টিপ: সেলাই করবেন না
বাট 11। n.s. এ একটি দম্পতিতে রূপান্তরের ভবিষ্যতে বিরল জলের আয়তন কত গুণ বৃদ্ধি করবে?
রাসায়নিক বিক্রিয়া জন্য aA + bB = cC + dD
ঘুম থেকে জাগা
de nA এবং nB হল মুক্ত বক্তৃতাগুলির সংখ্যা যা প্রতিক্রিয়া করেছে, ps এবং nD হল দ্রবীভূত পণ্যগুলির সংখ্যা, a, b, c এবং d হল স্টোচিওমেট্রিক সহগ৷
বক্তৃতার সংখ্যা থেকে, їх ভরে যাওয়া সহজ:
গ্যাসের মতো বক্তৃতার জন্য, তাদের বাধ্যবাধকতা বোঝাতে চি সেট করা আরও সাধারণ। যদি বিকারক এবং পণ্য ডি গ্যাস হয়, তাহলে এই বক্তৃতাগুলির হাড়ের সংখ্যা থেকে তাদের মধ্যে স্থানান্তর করুন:
![]()
vіdomih (প্রতি মন) পরিমাণ, মাসি বা বাধ্যতামূলক (গ্যাসের জন্য) একটি বক্তৃতা যা প্রতিক্রিয়ায় অংশ নেয়, অন্যান্য বক্তৃতার জন্য সমস্ত পরিমাণের মান নির্ণয় করা সম্ভব।
A এবং B গ্যাসের বিভিন্ন সমষ্টিতে, যার মধ্যে একটি প্রতিক্রিয়ায় অংশ নেয়, আপনি sp_v_dnoshnenja їkh obsyagіv VA: VB জানতে পারেন, এবং একটি প্রদত্ত sp_vv_dnoshnі - їkh obsyag sumіshi (বা navpaki)।
বাট rozvyazannya কর্ম
একটি উচ্চ তাপমাত্রায়, ম্যাগনেসিয়াম নাইট্রোজেনের সাথে বিক্রিয়া করে, আসুন আর্গনের সমষ্টি দেখে নেওয়া যাক, যার মোট আয়তন 5.6 l (n.o.) এবং 15 গ্রাম নাইট্রাইড যোগ করুন। প্রস্থান যোগফল V(N2): V(Ar) গ্যাসের আয়তন গণনা করুন।


জন্য টাস্ক স্বাধীন সমাধানঅংশ A
1. 6 লিটার নাইট্রিক অক্সাইড (II) 5 লিটার টকের সাথে বিক্রিয়া করে
2. একটি বন্ধ পাত্রে, 24 গ্রাম গ্রাফাইট 67.2 লিটার (n.a.) টক পুড়িয়ে দেওয়া হয়েছিল এবং টকের পরিমাণ সরানো হয়েছিল: পণ্যটি সমান
3. ওজোনেটরের মধ্য দিয়ে 7.5 মোল টক, যা প্রায়শই ওজোনে পরিণত হয়। "লবণ" (স্বাভাবিক মনের জন্য) 0.5 mol রক্তের জল (SO2 এ ফিরে যাওয়া) এর জন্য দাগ দেওয়ার পরে অবশিষ্ট থাকা; পরে, ওজোনিজার থেকে প্রস্থান করার সময় O3: O2 এর আয়তন হয়ে যায়
4. 142.8 গ্রাম ভরের পটাসিয়াম ব্রোমাইড, ক্লোরিনের সাথে সামান্য প্রতিক্রিয়া করার পরে, আমরা এটিকে 1 (ক্লোরিন): 2 (পুনরাবৃত্তি) ভলিউম্যাট্রিক অনুপাতের পুনরাবৃত্তির একই পরিমাণে গ্রহণ করব। গ্যালনি অবস্যাগ (লিটারে)
5. সুমিশ CH4 + H2 এর 17.92 l (n.o.) সম্পূর্ণ দহনের জন্য, 1 মোল টক প্রয়োজন ছিল। দিনের শেষে, CH4 এর মোট পরিমাণ: H2 আরও স্পষ্ট:
6. গ্যাস A, যখন অনুঘটকের উপর 0.04 mol KClO3 ভাজা হয়, তখন আমরা B গ্যাস দিয়ে পাত্রটি খুলে ফেলি, যেটি দেখা গিয়েছিল যখন আমরা জল দিয়ে 6 গ্রাম ক্যালসিয়াম পরীক্ষা করেছিলাম এবং A এর আয়তনের যোগফল নিয়ে গিয়েছিলাম: খ, সমান
7. পণ্যের সমষ্টির (নাইট্রোজেন, কার্বন ডাই অক্সাইড, জল) অতিরিক্ত অম্লতায় নাইট্রোবেনজিন থুতু ফেলার পরে, যার মধ্যে 4 লিটার (na) নাইট্রোজেন সরানো হয় এবং N2: O2 এর আয়তন 4: 1. লিটারের বেশি হয় , n u.) টক হয়ে যাওয়া
8. একটি স্টিলের বেলুনে 1 mol অ্যামোনিয়াম ক্লোরাইডের তাপ পচন করা হয়েছে, যাতে 11.2 লি (n.a.) অ্যামোনিয়াও থাকে। Kіntseve ob'єmne vіdnoshennia NH3: НCl dorovnyuє
9. সুমিশ টক এবং ক্লোরিন ভলিউম 9: 1 ভিকোরিস্তান KI এর পরিসর সহ 0.5 mol সাধারণ বক্তৃতা দেখার জন্য
10. কিসেনকে ওজোনেটরের মধ্য দিয়ে পাস করা হয়েছিল, যখন KClO3 এর 1 mol একটি অনুঘটকের উপর ভাজা হয়েছিল, যখন টকটির 5% ভাজা হয়েছিল, তখন টকটি ওজোনে পরিণত হয়েছিল এবং ওজোনেটর থেকে বের হওয়ার সময় O2: O3 এর আয়তন হ্রাস পেয়েছিল।
গ্যাস ফেজ থেকে পাতলা-গলিত ধাতু-পলিমার সিস্টেমের ছাঁচনির্মাণের ভৌত-রাসায়নিক নিয়মিততা
পাতলা-গলিত ধাতু-পলিমার উপকরণ (ধাতু পলিমার, পাতলা পলিমার আবরণ সহ ধাতব স্ল্যাব, সমৃদ্ধ বল সিস্টেম, ইত্যাদি), যা ভ্যাকুয়াম প্রযুক্তি দ্বারা ঢালাই করা হয়।
Si(100) পৃষ্ঠে Ge-এর এপিটাক্সিয়াল বৃদ্ধি
পাতলা স্লিক্সের পদার্থবিদ্যা থেকে, মাইক্রোইলেক্ট্রনিক্স, অপটিক্স, ফিটিং এবং নতুন প্রযুক্তির অন্যান্য গ্যাজেটগুলির আরও বিকাশের সম্ভাবনার নাগাল। ইলেকট্রনিক মাইক্রোমাইনিংয়ের সাফল্য...
উপাদানগুলি যা শক্তিশালী হতে পারে এবং পলিমার উপকরণগুলির দাহ্যতা কমাতে পারে
কিছুক্ষণ পরে, দেশের অর্থনীতি কয়েক মিলিয়ন রুবেল থেকে রক্ষা পাবে। পলিমারিক পদার্থ পোড়ালে দেখা যায় বড় সংখ্যাবিষাক্ত গ্যাস যা মানুষের জন্য ক্ষতিকর এবং...
পাঠের উদ্দেশ্য:
নথির জায়গায় পর্যালোচনা করুন
“রসায়ন ক্লাস 9 রাসায়নিক বিক্রিয়ায় নীল গ্যাসের আয়তন। রাসায়নিক সমতার জন্য গ্যাসের মোট খরচের হিসাব।
"রাসায়নিক বিক্রিয়ায় নীল গ্যাসের আয়তন" বিষয়ের রসায়ন পাঠ। রাসায়নিক সমতার জন্য গ্যাসের মোট খরচের হিসাব"
ক্রিটিকাল থট টেকনিকের পাঠ #3
পাঠের উদ্দেশ্য:জৈব বক্তৃতা রাসায়নিক বিক্রিয়া বাট থেকে গ্যাসের মত বক্তৃতা জন্য জল আয়তনের আইন সম্পর্কে জ্ঞান গঠন; rozrahunkіv іz khіmіchnyh rivnyan জন্য o'mnih spіvvіdnoshen আইন গঠন করুন। Dodoskonaljuvati vminnya uchnіv virіshuvati rozrakhunkovі zavdannya shdo rіvnyan khіmіchnih reaktsіy। বিকাশ vmіnnya uchnіv গুদাম khіmіchі zavdannya। সমালোচনামূলক চিন্তাভাবনা বিকাশ করুন। অবজেক্টটি শেষ না হওয়া পর্যন্ত একটি ইতিবাচক সেটিং গঠন করুন, টাস্ক শেষ হওয়ার আগে সেটিং এর একটি সমষ্টি।
মালিকানা:টাস্ক কার্ড।
লুকানো পাঠ।
আমি.গা গরম করা(শিক্ষার্থীরা তাদের চিন্তায় হারিয়ে যায়)
এ. ফ্রান্স "যদি একজন ব্যক্তি মনে করেন, তারা সুমনিভ হবেন না, তবে তারা মুগ্ধ হবেন না, যদি..."
আপনি কিভাবে এই বাক্যাংশ শেষ করেছেন?
দলবদ্ধভাবে অনুশীলন করতে শিখুন। প্রস্তাবিত বিকল্পগুলি লিখুন। tі চয়ন করুন, їhnyu dumku আরো মাপসই উপর yakі.
ভিসনোভোক: "যদি একজন ব্যক্তি মনে করেন, তারা বিভ্রান্ত হবেন না, তবে তারা যদি হয় তবে তাদের গাওয়া হবে না।"
আমি spodіvayus, ডানদিকে scho, যা আমরা পাঠে ব্যস্ত, আপনাকে আঘাত করতে এবং আপনি বর্তমান সময়ে আপনার প্রাণবন্ততা দেখাবেন।
২. শেখার কার্যকলাপ জন্য অনুপ্রেরণা.
স্তম্ভিত যারা পাঠ প্রধান.
S. আপডেটের ধাপ
V_den চিত্রের পিছনে alkenіv এবং alkіnіv এর রাসায়নিক শক্তি অনুমান করুন।
কেন তুমি পাত্তা দিও মোলার সংকোচন n.s জন্য যাই হোক না কেন গ্যাস.
পরামর্শ: 22.4 l/mol
Avogadro এর আইন কিভাবে প্রণয়ন করা হয়?
পরামর্শ:বিভিন্ন গ্যাসের একই বাধ্যবাধকতায়, একই মনের জন্য (t, p), একই সংখ্যক অণুর প্রতিশোধ নেওয়া হয়।
ভিসনোভোক:বিক্রিয়ায় গ্যাসের মতো বিকারক এবং দ্রব্যের পরিমাণ সমন্বিত হয় কারণ বিক্রিয়ায় তাদের সহগ সমান হয়। khіmіchnyh rozrahunkіv জন্য Tsya zakonіrnіst vikoristovuєtsya।
সৃজনশীল কাজ:(বিষয়টিতে পণ্ডিতদের শক্তিশালী জ্ঞানের সাথে আপনাকে পুনর্বিবেচনার সুযোগ দেয়)
তিনটি সংখ্যাযুক্ত টিউবে, স্টপার দিয়ে বন্ধ, є: মিথেন, ইথিলিন, অ্যাসিটিলিন। কীভাবে চিনবেন, গ্যাস কোথায় আছে?
IV. বিজ্ঞপ্তির ধাপ(বস্তুগত জ্ঞানে এনে, যা সমস্যার উপর ভিত্তি করে, সত্যের সন্ধান করুন)।
বক্তৃতাটি ("ক্যারোজেল" শক্তিশালী করা হয়েছে: বিয়ের দিন শুরুতে কীভাবে দেওয়া হয় তার প্রাথমিক ধারণা; শেষের পরে, শিক্ষার্থীরা একটি বাজিতে একত্রিত হয়, অনুরূপ কাজগুলি জিতে নেয়; একই রকম কাজগুলিকে একত্রিত করে, যেমন আদালতের দিন, ইত্যাদি .)
7 লিটার প্রোপেনের সাথে বিক্রিয়া করার জন্য ক্লোরিন (n.o.) এর আয়তন হল:
ক) 14 এল; খ) 10 লি; গ) 7 l; ঘ) 22.4 লিটার।
3. স্প্যালিং সুমিশির জন্য আপনার মোট টাকার পরিমাণ গণনা করুন,
এটি 5 লিটার ইথিলিন এবং 7 লি অ্যাসিটিলিন (এন.ও.) পর্যন্ত যোগ করে।
প্রতিক্রিয়া সমান না হওয়া পর্যন্ত 7 লিটার ইথিলিনের সম্পূর্ণ হাইড্রোলাইসিসের জন্য কী পরিমাণ জল প্রয়োজন তা অনুগ্রহ করে নির্দেশ করুন:
Z 2 H 4 + H 2 \u003d Z 2 H 6 a) 7 l; খ) 6 এল; গ) 14 এল; ঘ) 3.5 লিটার।
দম্পতিরা কাজ করে।শিক্ষার্থীরা, বাজিতে একত্রিত হয়ে, একত্রে অনুরূপ আদেশ দেয়, যেমন একটি বিরিশু সুদিন্ন্যা দম্পতি:
সম্পূর্ণ জল দেওয়ার জন্য প্রয়োজনীয় জলের পরিমাণ হল 15 লিটার বুটিন, আরও: ক) 15 লিটার; খ) 30 লি; গ) 7.5 লি; ঘ) 3.5 লিটার।
C 2 H 2 + 2Cl 2 \u003d C 2 H 2 Cl 2 বিক্রিয়ার উপর নির্ভর করে যেকোন আয়তনের ক্লোরিন 5 লি অ্যাসিটিলিনের সাথে যোগ করা হয়
ক) 5 এল; খ) 10 লি; গ) 2.5 লি; ঘ) 22.4 লিটার।
3. মোট খরচ গণনা করুন, কারণ এটি অতিরিক্ত ব্যয় করা প্রয়োজন
10 m3 অ্যাসিটিলিন (N.O.)।
ভি. প্রতিফলন
কার্ড থেকে Vikonannya টাস্ক.
জলের মোট পরিমাণ গণনা করুন, X এর বক্তৃতা বারবার জল দেওয়ার প্রয়োজন।
(সারণীটি পূরণ করতে স্বাধীনভাবে শিখুন, কাজ শেষ হওয়ার পরে, তারা প্রশ্নের উত্তর দেবে)।
| অবস্যগ বক্তৃতা X, l | বক্তৃতা সূত্র এক্স | রিভন্যান্ন্যা গিদ্রোভান্ন্যা | জল, ঠ |
|
ভিІ . পাঠ থেকে Visnovki
আসন্ন পাঠের কাজটি প্রণয়ন করা হয়েছে।
ভিІ আমি. পাঠের জন্য থলি
অষ্টম. বাড়ির কাজ
Propratsiuvati অনুচ্ছেদ 23, vikonati ডান দিকে 206, 207.