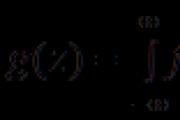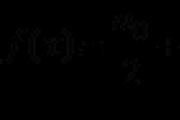Acerca de'єmni vіdnіnі gazіv en reacciones químicas. Ley de Avogadro
Molino de gasolina de Rechovin. Ley de Avogadro. Volumen molar de gas.
Los registros se pueden reconstruir en tres molinos de agregados: sólidos, duros y similares a gas. Las partículas, además, se almacenan en palabras sólidas, para terminar unidas motívamente entre sí, es decir, las palabras son firmes en forma singular. Las partículas de partículas sólidas pueden ser átomos, moléculas y pueden crear estructuras cristalinas. Muchas partes son propensas a una pequeña amplitud para las universidades de krats cristalinos. En la parte inferior de la partícula, uno está ligado con uno más débil y puede sobresaturarse para alcanzar una gran variedad. A eso, puedo ver la arruga e hinchar la forma del juez, en tal hedor de ser encontrado.
La transición del discurso de una estrofa sólida puede verse cuando se calienta, como resultado de lo cual la amplitud del número de partículas crece gradualmente. A la misma temperatura, las partículas del río se llenan de edificios, cuanto más alto es el grano, se agrega el derretido. Cuando hace frío, navpaki, las partículas de la línea toman el poder del cambio y se fijan en la posición de canto, estableciendo un discurso sólido. Para las mentes malvadas de los Ridin, como regla, dicen errores moleculares. A altas temperaturas, se puede utilizar la estructura de la línea (fusión de sales y metales).
Vzaєmodiya entre moléculas de nagato débil, menos iones en estructuras cristalinas iónicas; átomos unidos por un enlace covalente en estructuras atómicas; iones metálicos, unidos con gas electrónico en estructuras metálicas.
Nombraré el campo duro y aburrido del discurso molino de condensación... Los chilnosti de los ríos en el molino condensado son alrededor de 0.5-22.5 g / cm 3 en los límites. Las palabras en el molino similar a gas son significativamente menos eficientes - cerca de 10 –2 - 10 –3 g / cm 3. La transición de un molino a gas dará como resultado el calentamiento de las cámaras, que se encuentra en un molino condensado (una sublimación de cámaras sólidas). Parecido a un gas para las mentes malvadas del habla está compuesto de moléculas.
Durante la transición al molino similar a un gas, las partículas del habla se suman a la fuerza de la interacción intermolecular. Obsyag, que toma prestado gas, es, según el día, un espacio obsyag vilny entre las moléculas del gas, por lo que colapsará caóticamente. La magnitud del espacio comienza con la temperatura y el vicio. Con mucho dinero, nos ocupamos de las moléculas en sí mismas, podemos salirnos con la nuestra. zvidsey viplya Ley de Avogadro :
Para las mismas mentes, el mismo número de moléculas se vengará de las mismas mentes.
De la ley de Avogadro dos rastros principales .
Primer Slidstvo
Un mol de gas para las mismas mentes, tomando prestado el mismo obsyag. Tsey obsyag ser llamado por gas molar V metro ) , Varía en m 3 / mol (parcialmente en dm 3 / mol). Suministro de gas de Molyarny para el suministro de gas antes del último año:
Aparentemente, el valor de V m se deposita de las mentes (temperatura, vicio). Para la revisión de la planta, es necesario memorizar el valor de V m en mentes normales (n.o.) - vicio atmosférico (101,3 kPa) y temperatura del hielo (0 0 C o 273,15 K).
Para sumideros normales V m = 22,4 dm 3 / mol, abo
en unidades de СІ 0.0224 m 3 / mol.
Otro acierto
Los shilnosti de gases (para la mayoría de las mismas obligaciones) se establecen entre sí como masa molar de gases.
Tse se puede ver desde tal mіrkuvan. Nekhai dos porciones de gases jóvenes del mismo obsyagu (obsyagi vimiryana para las mismas mentes). Sabemos їх masi:
Sudario їх mas:
¿Qué tan victorioso es?
Detrás de la ley de Avogadro n 1 = n 2, estrellas:
Entrega de suministros de gas con la capacidad de un gas en términos de ( D ). D - el valor es adimensional.
Conociendo D y la masa molar de un gas, es fácil conocer la masa molar de un gas:
; M 1 = M 2 × D.
ponerse
M (x) = M (H2) × D = 2 × 8.5 = 17 g / mol
Gas de tal masa molar - amiak NH 3 .
La fuerza de un gas en un carbohidrato de dos personas. Tome la masa molar en carbohidratos.
La masa molar promedio es de 29 g / mol.
M (x) = M (punto de vista) × D = 29 × 2 = 58 g / mol
Un carbohidrato con tal masa molar es Z 4 H 10 butano.
Deslizar significa que el gas con una masa molar de menos de 29 piernas por bebida, más de 29 - importante.
Las empresas Rosrakhunkov pueden tener un tributo al nitrógeno, la acidez y el gas. En general, para el valor de la masa molar, es necesario multiplicar la cantidad de densidad por la masa molar basada en nitrógeno (28 g / mol), ácido (32 g / mol), etc.
La ley de Avogadro se usa ampliamente entre los químicos. Las oscilaciones de los gases son aproximadamente el número proporcional de conversiones, luego la eficiencia en la reacción eficiente, que muestra el número de reactivos, proporcional al número de gases convertibles. Obviamente, está bien ser vimirianos para las mismas mentes.
extremo
Yakiy obsyag kisnyu será necesario para dormir 2 dm 3 ¿propano? Obligaciones vimiryani para n. a.
Ç 3 Н 8 + 5О 2 3СО 2 + 4Н 2 О.
Según la ley de Avogadro, el mismo número de moléculas debería ser reemplazado por el mismo número de moléculas y, aparentemente, el mismo número de polillas de rechovinas. Tome propano por 1 dm3. Todi, con una reacción razonable, para 1 dm 3 de propano, se requieren 5 dm 3 de ácido y 2 dm 3 (dos litros) - 10 dm 3 Pro 2.
Khimiya
Química de zagalna
Comprensión básica, leyes y teorías de la química.
Acerca de'єmni vіdnіnі gazіv en reacciones químicas. Ley de Avogadro
Ley de Gay-Lussac sobre
Gazi reacciona como él mismo al cantar giros generales. U 1808 p. J.L. Gay-Lussac habiendo establecido el siguiente patrón: Los gases de Osyagi, que entran en reacción, transportan uno a uno y productos gaseosos de la reacción, que no son números muy grandes..
Damos una pista sobre la ley de vidomy en química yak la ley de B. Para ti, necesitas cuidar los gases, participar en la reacción, estar pendiente de las mismas temperaturas y vicios.
Los anuncios de comunicaciones de gas, que entran en una reacción química, se refieren a las relaciones de la economía, por ejemplo :.
En este vypadku reaccionan 3 volúmenes de agua con 1 volumen de nitrógeno, como resultado de lo cual se establecen 2 volúmenes de amoníaco, para mostrar el rendimiento.
Zavdannya. ¿Cuál es la cantidad de agua necesaria para la reacción con 2 m 3 de nitrógeno?
Decisión
De la reacción reaccionaria se desprende claramente que el volumen de agua es culpable de 3 veces más que el volumen de nitrógeno:
obsyag vodnyu m3.
Ley de Avogadro
Para aclarar las definiciones simples de gases reactivos, use la ley de Avogadro: Para las mismas mentes (temperatura y agarre), se produce el mismo número de moléculas en los intercambios regulares de pequeños gases.Debido a la ley de Avogadro, no bebí dos nicoli ese:
1) Un mol de gas para las mismas mentes del mismo préstamo.
Para mentes normales (n. U.), Tobto a una temperatura de 273 K y un vicio de 101,3 kPa (1 atm), 1 mol de cualquier préstamo de gas, volumen, rivny 22,4 litros. Tsey obsyag nombre gas molar me refiero a yak l / mol.
El intercambio molar se puede desarrollar para la fórmula.
.
2) Con un agarre constante, es probable que la temperatura del gas se vea privada de su masa molar.
Tse lo permite beca excepcional primer gas de una manera diferente:
,
Delaware D- Seguro, como les muestro, han desarrollado el primer gas que es importante para otros para las mismas mentes.
La mayoría de las veces, la permeabilidad a los gases es normal. Todi:
; .
Puedo rozrahuvati vіdnosnu gustina para el gas be-yaky.
Disponer de una amplia variedad de materiales chisme metódico"Empiece a resolver problemas desde la química". Autor - redactores: profesor de química de la categoría de alimentos, metodólogo. metodólogo del viddilu metódico inicial Establecer la educación "Grodno OIC y PRR y SV" Korobova N.P.
Cálculo del volumen molar de gases.
El cálculo del gas gustini dado.
Acerca de'єmni vіdnosini gazіv
Un lunar es como gas para las mismas mentes, ¿prestado? Entonces, para mentes normales (n.o.),tobto. a temperaturas і 0 ° С en un vicio atmosférico normal, que cuesta 101,3 kPa, un mol de un préstamo a un gas22,4 dm 3.
SantuarioCalentaré el gas hasta una cantidad química específica de habla є el valor, que se llamapor gas molarV m):
V m = V/ nortedm 3, estrellasV = V m · norte
Para ello, es importante tener un gas ligero o importante, pero no suficiente;
r 1 / r 2 = M 1 V 1 / M 2 V 2 = M 1 / M 2 = D 2.Se puede ver a la vista del viraz inducido: la cantidad de producción de gas, la cantidad de peso molar.
La relación entre la masa molar de un gas y la masa molar de un gas.
de buena fe ( D 2 ) un gas de un gas.Conociendo la especificidad de un gas en términos de su valor, es posible determinar el valor de su masa molar:
METRO
1 = METRO 2 · D 2 .Por cierto є mucho gas, eso con un volumen de 22,4 litros. El valor es numéricamente alto:
M pov. = 29 g / mol
Según la ley de Avogadro, el número de moléculas de diferentes gases es el mismo para la tranquilidad de las mentes que piden prestada la misma cantidad.
De tsyogo vyplya otro sabor.
A temperaturas constantes, el agarre de un gas entra en la reacción de los gases, uno a uno, y también a una gran cantidad de productos similares a los gases, que se establecen, como un pequeño número de números.
La ley del balón fue formulada por Gay-Lussac como la ley del derecho consuetudinario. En tal rango, si una reacción química tiene mucho que ver con un habla similar a un gas, entonces para una reacción ordinaria es posible establecer mucha evidencia.
Osyagi gases, scho reaccionan y obsesionan, proporcional a la química del número de palabras:
V 1 / V 2 = n 1 / n 2 tobto. V 1 y V 2
coeficientes numéricamente iguales en una reacción igual.stock 1. Balon vm_shchuє 0,5 kg de agua comprimida. Yakiy ob'єmel prestamo son tantos? Umovi normal.
Decisión:
1. Numerosos productos químicos
vodnu, cómo vengarse en balony:norte
(H 2) = 500/2 = 250 (mol), de M (H 2) = 2 g / mol.2.Oskilka para mentes normales 1 mol be-like gas préstamo obsyag 22.4
dm 3, luegoV = V m · norte, V( H 2 ) = 22,4 * 250 = 5600 (dm 3)
Tipo: 5600 dm 3
Trasero 2. Almacén de yaks (en%) de aleación de aluminio-aluminio, cuando se muestreó 1 g de demasiado ácido clorhídrico y se observaron 1,18 l vodnu?
Decisión:
1.Osks en la reacción con ácido ingrese solo aluminio, luegoanote:
2A1 + 6HC1 = 2A1C1 3 + 3H 2
2 mol 3 mol
2.Numerable calidad alegre vodnyu:
norte(H 2 ) = 1,18 / 22,4 = 0,05 (mol)
3.Según la reacción igual, se calcula la cantidad de aluminio,cómo vengarse en el rafting:
3 mol 2 mol de aluminio
0,05 mol Ya veo, voy a reaccionarXmol de aluminio
x = 0.05 2/3 = 0.033 (mol),
metro( Alabama) = 0.03527 = 0.9 (g), de M (Al) = 27 g / mol
5. Numerosos mucho aluminio en metal:
w(Al) = metro ( Alabama ) / metro (Aleación) , w( A1) = 0,9 / 1 = 0,9 y 90%.
Todi masova parte de aleación midi u 10%
Tipo: 90% aluminio, 10% medio
stock 3. Visibilidad a la validez:b) en agua con dióxido de carbono.
Decisión:
1. Se sabe que la suerte de los niños es:
D povit (Aproximadamente 2) =METRO(Pro 2) /METRO (pov.) = 32/29= 1,1.
2.Inicialmente, la densidad en dióxido de carbono por vodnu
D H2 (CO 2) =METRO(Ç 2) /METRO(H2) = 44/2 = 22.
Ver: 1,1; 22
stock 4. Visite el volumen de sumas de gases, que se pueden almacenar en 0,5 mol de ácido, 0,5 mol de agua.que 0.5 mol en dióxido de carbono.
Decisión:
1. Se conoce la química de la cantidad de gas:
norte(suma) = 0.5 + 0.5 + 0.5 = 1.5 (mol).
2. Cantidad calculada de sumas de gas:
V(suma) = 22,4 * 1,5 = 33,6 (dm 3).
Tipo: 33,6 dm 3 suma
Trasero 5. Rompe el volumen en dióxido de carbono, cuando quemas 11,2 m 3 metano CH 4.
Decisión:
1. Registro de la reacción química de la minería de metano:
CH 4 + 2O 2 = CO 2 + 2H 2 O
1 Topo1 Topo
1 m 3 1 m 3
2. Para el cálculo de la cantidad de dióxido de carbono en el almacén, se almacena en la misma proporción:
cuando duerme 1 m 3 СН 4 vide 1 m 3 2
al dormir 11,2 m 3 CH 4 Wiide x m 3 2
x = 11,2 1/1 = 11,2 (m 3)
Vista: 11,2 m 3 en dióxido de carbono
Trasero 6. El cilindro de acero para exprimir los gases exprimidos se almacenó con un peso de ácido picante de 8 kg.
¿Qué tipo de préstamo obsyag de una planta de gas (n.o.)?
Decisión:
1. Numerosos números químicos de la cereza ácida nativa:
norte( O 2 ) = 8000/32 = 250 (mol).
2. Numerosos obsyag gazopodіbny kisnyu:
V( O 2 ) = 22,4250 = 5600 dm 3.
Tipo: 5600 dm 3
Trasero 7. Calcule el peso del volumen con un volumen de 1 m. 3 (n.u.), hay 78 partes voluminosas de nitrógeno, 21 - ácido, 1 - argón (excepto esos gases).
Decisión:
1. Eche un vistazo a la fábrica, pague el gas en cada turno del día:
V( norte 2 ) = 1 · 0,78 = 0,78 m 3;
V(Aproximadamente 2) = 1 0,21 = 0,21 m 3
V(Ar) = 1 · 0.01 = 0.01 m 3.
2. Numerosas cantidades químicas de gas cutáneo:
norte( norte 2 ) = 0,78 / 22,4 · 10-3 = 34,8 (mol),
norte(Aproximadamente 2) = 0.21 / 22.4 · 10-3 = 9.4 (mol),
norte(Ar) = 0,01 / 22,4 · 10 -3 = 0,45 (mol).
3. Numerosas masas de gas:
metro(norte 2 ) = 34,8 28 = 974 (g),
metro(Sobre 2 ) = 9,4 32 = 30 (g),
metro(Ar) = 0,45 40 = 18 (d).
4. Numerosos masu povitrya:
metro(Povitrya) = 974 + 301 + 18 = 1293 (g) o 1,293 kg.
Tipo: 1.293 kg por hora
Trasero 8. Cuando se agrega al medidor, la cantidad de agua es de 0.1 m 3 el volumen de la suma cambió en 0.09 m 3 .
Yaki obsyagiagua y matón agrio en las sumas malvadas, ¿cómo se quema el gas, que se está desbordando (n.e.p.)?
Decisión:
1. Anote la reacción:
2H 2 + Sobre 2 = 2H 2 Sobre
2 mol 1 mol 2 mol
2. Visnachaєmo obsyagi gas, scho entró en la reacción.
obsyag La conmoción del gas se apresuró para la aprobación del agua salvaje, por lo que una gran cantidad de gas, que entró en reacción, costó 0.09 m 3 .
Porque Gazi entrar en la reacción 2: 1, luego s 0.09 m 3 dos partes
caer en el agua, y uno - en kissen. Otzhe, en reacción
ingresado 0.06 m 3 profundidad del agua 0.03 m 3 Me estoy agriando.
3. Numerosos obsyagi de gases en las sumas perversas.
Porque el gas, que se ve ensombrecido, se quema, luego el precio de un día es de 0.01 m 3 .
V(H 2 ) = 0.01 + 0.06 = 0.07 (m 3 ) unos 70 l,
V(Sobre 2 ) = 0,1 - 0,07 = 0,03 (m 3 ) o unos 30 litros.
Tipo: 70 litros de agua, 30 litros de agua
Trasero 9. ¿Por qué querría almacenar hasta 56 litros de argón y 28 litros de nitrógeno (n.e.p.)?
Decisión:
1. Vyhodyachny viznennya vіdnosі gustini gazіv,
D H 2 = METRO (resumen) / METRO(H 2 ).
2. Numerosas cantidades químicas de la misma cantidad de gas:
norte(Arkansas) = 5,6 / 22,4 = 2,5 (mol);
norte(norte 2 ) = 28 / 22,4 = 1,25 (mol);
norte(suma) = 2.5 + 1.25 = 3.75 (mol).
metro(Arkansas) = 2,5 40 = 100 (g),
metro(norte 2 ) = 1,25 28 = 35 (g),
metro(resumen) = 100 + 35 = 135 (g), porque
M (Ar) = 40 g / mol, M (norte 2 ) = 28 g / mol.
3. Masa molar calculada de la suma:
M (resumen) = metro (resumen) / norte (resumen) ;
M (resumen) = 135 / 3.75 = 36 (g / mol)
4. El valor numérico de la cantidad de gas en el agua es:
D H 2 = 36/2 = 18.
Vista: 18
stock 10. ¿Cuánto puedo quemar 3 g de madera de un trilithrovy banci, que recuerda a sour (n.u.)?
Decisión:
1. Registro de la reacción de la mina vugilya:
Z + Sobre 2 = CO 2
1 mol 1 mol
2. Numerosos números de química de vugilya:
norte(CON) = 3/12 = 0,25 (mol), por tanto M (C) = 12 g / mol.
Una buena cantidad de ácido, necesario para la reacción, si también es necesario. 0,25 mol (basado en la reacción típica).
3. Se requiere un gran volumen para dormir 3 g de vugil:
V(O 2 ) = 0,25 22,4 = 5,6 (l).
4. El gas Oskilki se toma prestado por la cantidad de juicio, en el que se encuentra, є 3 litros de ácido. Otzhe, tsієї kіlkostі no silba para dormir 3 g de lana.
Mira: no mezclar
stock 11. ¿Le gustaría desarrollar mucha agua fértil y un par de veces cuando es normal?
Para una reacción química aA + bB = cC + dD
aparecer
de nА y nВ - una serie de discursos desordenados que entraron en la reacción, pS y nD - una serie de productos que fueron aprobados, a, b, c і d - rendimiento estequiométrico.
A partir del número de palabras, es fácil pasar a їх masa:
Para los discursos de gas, a menudo es necesario establecer el número de veces. Si el reactivo y el producto D son gases, entonces la transición se lleva a cabo del número de palabras al número de intercambios:
![]()
Para vіdomih (para la mente) de unos pocos, y por mucho dinero (para el gas) uno de los discursos, para que podamos participar en la reacción, es posible desarrollar el significado de todos los valores para el otros discursos.
Si tiene muchos gases A y B, uno de ellos tomará el destino de la reacción, puede saber tomar la relación de estos informes VA: VB, y a un ritmo determinado, los de las partes (o navpaki).
Problemas de resolución de glúteos
A altas temperaturas, el magnesio reacciona con el nitrógeno, a partir de la suma con el argón, en un volumen de 5,6 l (n.u.) y 15 g de nitruro. Proteja la información sobre V (N2): V (Ar) en el estado actual de las cosas.


Zavdannya para solución independiente parte A
1. Reaccionaron 6 litros de óxido de nitrógeno (II) a partir de 5 litros de ácido (obshy; vimiryana para mentes ryvnyh), también, en la última suma, alrededor de una
2. Quemaron 24 g de grafito en 67,2 litros (n.u.) en un recipiente cerrado, y me lo quitaron.
3. Pasó por el ozonizador 7.5 mol amargo, que en parte está re-retocando con ozono. Crecimiento remanente de vitracción para "spalyuvannya" (para mentes normales) 0,5 mol de agua (para transformar en SO2); A partir del mismo tiempo, la cantidad de entrada de O3: O2 en las salidas del ozonizador se convirtió en
4. Se hizo reaccionar bromuro de calcio con una masa de 142,8 g sólo en el intervalo de cloro, extraído de una gran cantidad de alimentos en la cantidad de 1 (cloro): 2 (tal vez). Zagalny obsyag (en las letras) del vikhіdnoї sumіshі gazіv buv
5. Para una combustión adicional de 17,92 l (n.u.) de CH4 + H2 suma, se necesita 1 mol de ácido. A las sumas actuales sobre mí, la entrega de CH4: H2:
6. El gas A, mientras fríe 0.04 mol de KClO3 en el catalizador, perdió (en n., Pivnim
7. La obtención del nitrobenceno en exceso de acidez se toma de la cantidad de productos (nitrógeno, gas dióxido de carbono, agua), en los que se reemplazan 4 litros (na) de nitrógeno y la cantidad de N2: O2 se suministra a 4: 1 litros ... y.) amargo, volviéndose
8. Se llevó a cabo la distribución térmica de 1 mol de cloruro de amonio en un globo de acero, así como 11,2 litros (estándar) de amonio. Kintsev sobre'єmne vіdnoshennya NH3: НCl dorіvnyu
9. Sumy sour y cloro con rendimiento volumétrico 9: 1 vikoristan para ver 0,5 mol de habla inactiva para el rango KI, de la misma fuente de información (en litros, n. U.)
10. Se pasó kisina a través del ozonizador, cuando se frió 1 mol de KClO3 sobre el catalizador, al 5% el ácido se convirtió en ozono y, en las salidas del ozonizador, se eliminó la cantidad de O2: O3.
Leyes fisicoquímicas de la formación de sistemas de metal-polímero de fusión fina a partir de la fase gaseosa
Materiales metal-poliméricos de fusión fina (polímeros metalizados, metal-virobi con recubrimientos poliméricos delgados, sistemas bagato-ball, etc.), que se moldean mediante tecnología de vacío.
Crecimiento epitaxial de Ge en la superficie de Si (100)
Con la física de las delgadas volutas de atar y las perspectivas para el desarrollo de la microelectrónica, la óptica, las adaptaciones y otros galuzei de la nueva tecnología. Éxitos mikrominiaturizatsii elektron ...
Componentes que pueden reducir el poder para reducir la combustibilidad de materiales poliméricos
Shoroku puede comenzar la economía de la tierra de los empresarios con cientos de millones de rublos. Al quemar materiales polidimensionales, consulte Gran numero gases tóxicos, suciedad en las personas y ...
Propósito de la lección:
Revisión del documento
“Química novena clase. Enumeración de spіvvіdnoshennі gazіv común para chemіchnіy іvnyannyi.
Una lección de química sobre el tema “Acerca de los gases comunes en las reacciones químicas. Enumeración de spіvvіdnoshennі gazіv común para chemіchnіy іvnyannyi "
Lección n. ° 3 para la técnica de falta crítica
Propósito de la lección: la formulación del conocimiento sobre la ley de las denominaciones comunes para el habla gaseosa con el foco de reacciones químicas del habla orgánica; formovati vminnya zastosovuvati la ley de amnistía spіvvіdnoshen para rozrahunіv si chemіch pіvnyany. Sin lugar a dudas, en la lista de científicos, virishuvati rozrakhunkovs se han desarrollado y preparado para el desarrollo de reacciones químicas. Desarrollo de científicos, almacenamiento de plantas químicas. El desarrollo es más crítico que la misión. Formuvati se coloca positivamente antes del sujeto, se coloca sumariamente antes del sujeto.
Posesión: card-zavdannya.
Ve a la lección.
I.Calentamiento(Aprendiendo a perderme antes de captar mis pensamientos)
A. Frans "Si malinterpretas un lyud, no se ganará, se ganará cerveza, si ..."
Yak bi vee terminó la frase qiu?
Práctica de aprendizaje en grupos. Anote las opciones propuestas. Vibra eso, a medida que vayas pensando más en tus pensamientos.
Visnovok: "Si te perdiste un lyudin, no lo conseguiré, no me sentiré honrado si no lo hiciera".
Me alienta, a la derecha, ya que estoy involucrado en el curso, a vincularlos y ver su salud y memoria.
II. Motivación por el desempeño educativo.
Aturdido por aquellos que zavdan lección.
Sh. Paso de actualización
Para el Diagrama El Día de la Decisión de la Química de la Autoridad de Alkeny y Alkeniv.
Qué está pasando intercambio molar ser como gas para n.u.
Vista: 22,4 l / mol
¿Cómo se formula la ley de Avogadro?
Vista: El mismo número de moléculas para las mismas mentes (t, p) tiene el mismo número de moléculas.
Visnovok: La cantidad de reactivos similares a gases y los productos de la reacción se utilizan para reducir la eficacia de la reacción. Es una regla general salir victorioso de los proyectos de química.
Zavdannya creativo:(Sí, puede pasar al conocimiento serio de los académicos sobre el tema)
En tres tubos de ensayo numerados, sellados con tapones, є: metano, etileno, acetileno. ¿Qué tipo de gas hay?
IV... La etapa de aprendizaje(Llevar al conocimiento del material científico, cómo girar en espiral sobre el problema, el chiste de la verdad).
La conferencia se fortaleció ("Carrusel": la comprensión básica se le da a la escuela;
Sobre el cloro (n.u.), que entra en la reacción con 7 litros de propeno, dorіvnyuє:
a) 14 l; b) 10 l; c) 7 l; d) 22,4 litros.
3. Calcule la cantidad de dinero que necesita para dormir,
almacenar para 5 litros de etileno y 7 litros de acetileno (n.o.).
Cabe señalar que el volumen de agua es necesario para la hidratación adicional de 7 litros de etileno, siempre que la reacción sea correcta:
Z 2 H 4 + H 2 = Z 2 H 6 a) 7 l; b) 6 l; c) 14 l; d) 3,5 l.
El robot está en parejas. Los científicos, reunidos en una apuesta, almacenarán algunos empleados más, como último par:
El volumen de agua necesario para la hidratación repetida de 15 litros de butino, para la entrega: a) 15 litros; b) 30 l; c) 7,5 l; d) 3,5 l.
Se usa un cierto volumen de cloro hasta 5 litros de acetileno, de hecho antes de la reacción С 2 Н 2 + 2Cl 2 = С 2 Н 2 Cl 2
a) 5 l; b) 10 l; c) 2,5 l; d) 22,4 litros.
3. Cuente la cantidad de dinero, ya que es necesario vitrar para la salvación.
10 m3 de acetileno (n.o.).
V... Reflexión
Visitando la tarjeta.
Calcule la cantidad de dinero necesaria para el apoyo general del discurso de H.
(Científicamente de forma independiente zapovnyayut la tabla, cuando el robot esté terminado, se mostrará).
| Obsyag discurso X, l | Fórmula del habla X | Rivnyannya gidruvannya | vodnyu, l |
|
VІ ... Visnovki en la lección
Formulación de una lección ofensiva.
VІ I... Bolsas para una lección
VIII... Inicio zavdannya
Continúe con el párrafo 23, la viconati derecha 206, 207 en el lateral.